В прошлых статьях я уже неоднократно приводил аргументы в пользу того, что одним из самых древних метаболических циклов мог быть ацетогенез на основе реакции 2CO + 2H2 => CH3COO(H). В настоящее время угарный газ (CO) практически полностью отсутствует в земной атмосфере, поэтому, без CO дегидрогеназы, восстанавливающей углекислый газ (CO2) до угарного не может обойтись ни одна бактерия или архея "исповедующая" ацетатный цикл. Однако, миллиарды лет назад земная атмосфера (или атмосфера другого космического тела, на которой возникла жизнь) была ещё не "испорчена" обильно выделяемым цианобактериями кислородом, и, соответственно, могла содержать CO в ощутимой концентрации. Указанная реакция примечательна тем, что совмещает в себе фиксацию углерода (из неорганического вещества - двух молекул угарного газа и двух молекул водорода получается одна молекула органического вещества - ацетата) с попутным запасением свободной энергии в фосфатной связи, например, в виде АТФ. Насколько мне известно, совмещение указанных двух базовых функций живых систем в одной реакции является своего рода уникальным явлением. И именно оно как нельзя лучше подходит для возникновения жизни, ибо позволяет совместить два последовательных шага эволюции в одном, что резко повышает вероятность "революционного прорыва".
Попробуем прикинуть, как именно могла выглядеть первая (или, по крайней мере, одна из первых) метаболическая цепочка в живых системах. У современных ацетогенов заключительные этапы реакции выглядят так:
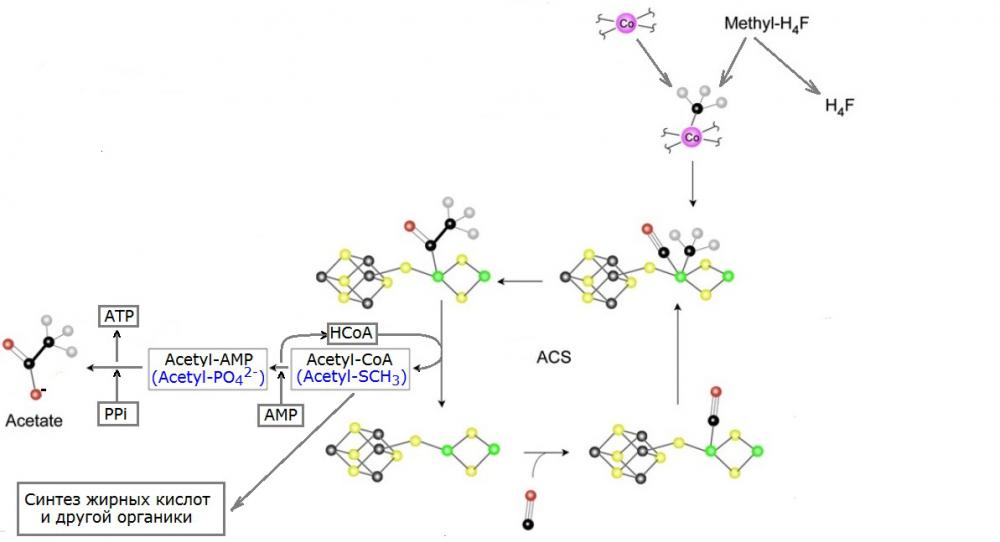
Рис. 1. Заключительные реакции ацетатного цикла (путь Вуда-Люнгдала) у бактерий (адаптировано из рисунка отсюда). Атомы различных химических элементов условно обозначены в виде шариков, окрашенных в следующие цвета: железо - серый, сера - жёлтый, никель - зелёный, углерод - чёрный, кислород - красный, кобальт - фиолетовый.
Как видно из рисунка, синтез ацетильной группы фактически осуществляется на фрагменте кристалла, содержащего атомы железа, серы и никеля. Минералы, в которых встречаются кристаллы подобного состава, носят общее название пентландиты, и они достаточно широко распространены в природе. Сама кристаллическая структура, играющая роль каталитического центра реакции, заключена внутри протеинового комплекса, называемого acetyl-CoA synthase, сокращённо ACS. Соответственно, все фазы работы состоящего из неорганики каталитического центра изображены на рисунке вокруг надписи ACS. Слева-внизу от неё показано исходное состояние наноразмерного "четырёхтактного двигателя". На первой фазе его работы к одному из атомов никеля присоединяется молекула угарного газа. В настоящее время его уже практически не осталось в атмосфере, поэтому, ацетогены вынуждены сами его синтезировать путём восстановления CO2 в другом реакционном центре - CO dehydrogenase (сокращённо COD) с последующей передачей в каталитический центр ACS по специально выделенному "туннелю", соединяющему оба протеиновых комплекса (это нужно для того, что бы синтезированный отнюдь не без усилий угарный газ никуда не "сбежал", и не окислился по дороге, ненароком, обратно в CO2). Однако, миллиарды лет назад угарного газа в атмосфере должно было быть гораздо больше, и он мог, в принципе, черпаться из окружающей среды напрямую. На второй фазе работы каталитического центра к тому же атому никеля на ещё одну пока свободную его валентность "подвешивается" метильная группа CH3, синтезированная ранее в другой цепочке реакций, и сданная "до востребования" на хранение атому кобальта (см. верхнюю-правую часть рисунка). Кстати, по странному, на первый взгляд, стечению обстоятельств, кобальт тоже является типичной (если не сказать обязательной) минорной примесью всё того же пентландита, см., например, английскую статью про него в википедии. Насколько мне известно, перенос метильной группы с кобальта на никель, то есть, напрямую с одного металла на другой, вообще является уникальной для живых систем химической реакцией. На третьем такте работы химического реактора CO и CH3 объединяются в ацетил, который по прежнему удерживается на атоме никеля (см. изображение соответсвующего состояния коэнзима слева-вверху относительно надписи ACS). Наконец, в заключительной фазе цикла ацетил отсоединяется от никеля и присоединяется к коферменту А приводя, тем самым, систему в исходное состояние. Что же касается судьбы ацетила, то она может быть различной. Как правило, он либо участвует в синтезе жирных кислот и другой органики, либо окисляется до ацетата с попутным запасением клеткой энергии в форме АТФ. На основе вышеизложенного, можно сделать вывод о том, что важнейшую роль в заключительных реакциях метаболического цикла ацетогенов играют кобальт и кристаллическая структура, включающая серу, железо и никель. Как уже отмечалось выше, все перечисленные химические элементы встречаются вместе в минерале пентландит, обнаруживаемом в породах, образовавшихся в результате магматических извержений, а так же в метеоритах (в частности, он встречается в составе наделавшего недавно много шума челябинского метеорита). Таким образом, не лишено оснований предположение, что исходно данные реакции могли идти на поверхности минералов (пусть и с гораздо меньшим КПД) даже абиогенно, а появившиеся позже органические кофакторы и протеиновые комплексы просто позволили взять их под контроль и использовать с выгодой для живых организмов. Возможность протекания абиогенного аналога реакции косвенно подтверждается и опытами Вэхтерсхойзера в которых при пропускании CO и H2S через воду, в которую был добавлен порошок, содержащий сульфиды железа и никеля, образовывался ацетат. Более того, как ещё один продукт реакции был зафиксирован метантиол, который может рассматриваться как простейший древний аналог кофермента А, осуществляющего последнюю реакцию в обсуждаемой цепочке (данный вариант с его продолжением, заключающимся в образовании активированного ортофосфатом ацетила, обозначен на Рис. 1 синим цветом). Но, оказывается, и это ещё не всё! В качестве бесплатного бонуса теории первичности ацетатного цикла можно рассматривать тот факт, что реакция образования ацетил-фосфата, являющаяся ключевой для синтеза АТФ на последнем этапе, существенным образом усиливается в присутствии калия, и, наоборот, подавляется в присутствии натрия. Это может быть одним из возможных объяснений до сих пор во многом загадочного стремления любой клетки поддерживать в своей цитоплазме неестественное для неживой природы соотношение концентраций калия и натрия. Внутриклеточное превалирование калия над натрием может быть своеобразным "родимым пятном", доставшимся живым системам в наследство ещё от самых ранних этапов их эволюции.
Если неорганические коферменты на первых порах действительно были главными действующими лицами развития биологических систем, резонно задать вопрос, почему для связывания метильной группы был выбран именно кобальт? Возможный ответ заключается в его магнитных свойствах. Как известно, к ферромагнетикам относятся железо, никель и кобальт, то есть, как раз те три металла, которые входят в состав комплекса ACS. Чем же ферромагнитизм может помочь в абиогенном синтезе органики? Известно, что намагниченные ферромагнетики создают вокруг себя магнитное поле. Это поле, в свою очередь, влияет на ориентацию полярных молекул. Угарный газ, сероводород, да и сам синтезируемый ацетат, все они являются как раз типичными полярными молекулами, и по этой причине в магнитном поле они будет ориентироваться вполне определённым образом. Предположим, что порода была намагничена внешним полем (это может быть, например, геомагнитное поле). Полярные органические молекулы, расположенные вблизи намагниченной породы, будет иметь преимущественное направление ориентации, определяемое направлением создаваемого ею магнитного поля. Это обстоятельство может хотя бы частично компенсировать отсутствие у неорганических кофакторов способности катализировать нужные реакции за счёт оптимального взаимного расположения взаимодействующих молекул, присутствующей у протеинов. Кстати говоря, недавно опыты по синтезу простой органики из CO и H2S были повторены другой группой учёных, использовавших в качестве катализатора только никель. Они, в основном, подтвердили результаты Вэхтерсхойзера, в частности, уже через несколько часов в растворе обнаруживаются ацетат и другие простые органические молекулы, содержащие метильную группу CH3. Таким образом, при условии непрерывной "подкачки" в систему угарного газа и сероводорода, например, вместе с вулканическими газами, недостатка в метильных группах, которые могут "оседать" на том же кобальте, или, даже, напрямую на никеле, по идее, быть не должно. Учитывая, что метильные группы современными прокариотами синтезируются из углекислого газа и водорода в результате сложного, многоэтапного процесса, включающего минимум 6 различных реакций, а так же то, что они тесно вовлечены в самые базовые биологические процессы, становится понятным то значение, которое имеет обнаруженный механизм их простого абиогенного синтеза.
Тем не менее, вулканические газы не самый надёжный источник, и для большей эффективности и устойчивости живым системам было бы весьма полезно научиться получать метильные группы так же и другими способами. И здесь можно присмотреться к любопытному экспериментальному факту - формальдегид способен спонтанно вступать в абиогенную реакцию с тетрагидрофолатом. По мнению многих исследователей, в условиях ранней восстановительной или нейтральной атмосферы такое простое вещество, как формальдегид, с химической формулой COH2, должно было синтезироваться в значительных количествах, обнаруживается он и в составе вещества комет. Тетрагидрофолат (на Рис.1 обозначен как H4F) является непременным участником многих реакций, происходящих при круговороте основных "кирпичиков" жизни - амино и нуклеиновых кислот. Это говорит о его вероятном появлении на сцене уже на самых ранних этапах эволюции живых систем. В контексте же данной статьи нас интересует прежде всего функция тетрагидрофолата как молекулы, служащей местом поэтапной сборки метильной группы, которая впоследствии входит в состав синтезируемого в обсуждаемой цепочке ацетата (у архей практически те же операции производятся на родственном тетрагидрофолату коферменте тетрагидрометаноптерине (H4MPT)). Соответственно, можно предположить, что между самым ранним вариантом с прямым перехватом кобальтом метильной группы от простых неорганических молекул, и современной достаточно сложной схемой её сборки на содержащих птерин коферментах, существовала ещё как минимум одна (но, скорее всего, конечено, гораздо больше) промежуточная ступень. На этом этапе формальдегид реагировал с птерином (точнее говоря, с парой атомов азота, один из которых входил в состав птерина, а другой располагался рядом с ним, см. Рис. 2 ) в результате чего оседал на соответствующем кофакторе (тетрагидрофолате или тетрагидрометанртерине) в виде метилена (CH2), а в качестве побочного продукта выделялась вода.
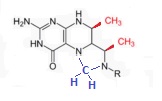
Рис. 2. Фиксация метилена (обозначен синим цветом) на содержащих птерин коферметах. Красным цветом обозначены метильные группы, присутствующие у тетрагидрометанртерина, но отсутствующие у тетрагидрофолата.
Как нетрудно заметить, птерин весьма напоминает одно из стандартных азотистых оснований - гуанин, отличаясь от него, по сути, лишь дополнительным атомом углерода в одном из своих гетероциклических колец. Подобные достаточно простые органические структуры должны были в больших количествах синтезироваться в среде, являющейся "колыбелью" жизни. Далее вступала в игру их конкуренция, и сохраниться в итоге смогли лишь те из них, которые тем или иным образом участвовали в автокаталитических циклах самовоспроизведения системы, являющихся, можно сказать, основным двигателем добиологического естественного отбора. Очевидно, что если содержащие птерин молекулы способствовали аккумуляции в системе свободной энергии в виде АТФ или других веществ, содержащих высокоэнергетичные фосфатные связи, то у них были очень хорошие шансы пройти предбиологический отбор и впоследствии быть включёнными в первые биологические метаболические цепочки. Так или иначе, но для того, что "застрявший" между двумя атомами азота метилен превратился в метильную группу, он должен присоединить ещё один атом водорода. У современных бактерий его компоненты (один протон и два электрона) к птерину доставляют молекулы кофермента NAD, а у архей (два протона и два электрона) - кофермерта F420. Любопытно, что в активном центре протеина, катализирующего у бактерий обсуждаемую реакцию (он называется метилентетрагидрофолатредуктаза) находится кофермент FAD, в состав которого, так же, как и в состав архейного "подносчика материала" для сборки атома водорода кофермента F420 входит флавинмононукдеотид (FMN). Как видим, спектр использующихся на последних этапах ацетатного цикла стандартных органических "кирпичиков" весьма ограничен, в частности, в различных сочетаниях в нём то и дело встречаются птерин, аденин, флавин, фосфаты, остатки аминокислот (например, в состав кофермента А входит остаток аланина) и т.д. При этом, почти у каждого кофермента на одном из его концов находится циклическая структура, способная комплиментарно взаимодействовать с одним или более стандартными нуклеотидами. В частности, птерин может комплиментарно взаимодействовать с аденином, FAD c цитозином и гуанином, NAD c цитозином, уридином и гуанином, F420 с цитозином. Всё это можно рассматриваить как очередной намёк на существование на самых ранних стадиях эволюции некого этапа, который можно условно назвать "миром коферментов". На этой стадии отбор первых органических молекул шёл по лёгкости их абиогенного синтеза, способности к участию в автокаталитических циклах, подерживающих их самовоспроизводство, а так же обеспечению устойчивости этих метаболических циклов к возможным изменениям условий внешней среды, способности к физико-химическому взаимодействию между собой, и на этой основе построению систем более высокого уровня сложности (тех же рибозимов, простых пептидных комплексов и т.д.). Роль "памяти" системы на данном этапе мог играть сам набор из нескольких десятков простых органических молекул, участвующих в автокаталитических циклах самовоспроизводства, а роль мутаций играли небольшие изменения структуры отдельных коферментов (например, метилирование, аминирование, добавление гидроксильных групп и т.д.), а так же случайные выпадения отдельных коферментов из пула и появление в нём новых органических молекул.
Но для того, что бы между различными вариантами самореплицирующихся систем могла существовать конкуренция, они должны быть физически отделены друг от друга, формируя квазинезависимые сообщества. Относительно способа подобного отделения существуют по крайней мере две различные точки зрения. Последователи одной из них в качестве отдельных микросистем, в которых шла предбиологическая эволюция, предлагают ячейки на дне океана (или другого водоёма), стенки которых образованы сульфидами железа, никеля и, возможно, ряда других веществ (существует сразу несколько разновидностей теорий, в которых взята за основу данная идея). Подобные структуры, напоминающие соты с характерным размером ячейки порядка сотых долей миллиметра, часто образуются в местах выхода магматического вещества (лава, раскалённые газы) на поверхность. Одним из самых горячих сторонников подобного сценария является шотландский исследователь Майкл Рассел. Альтернативой теории железно-никелево-серных "сот" на дне водоёмов выступает гипотеза о том, что строение протоклетки с самого начала напоминало структуру современных клеток, то есть, представляло из себя небольшие наполненные водной пузырьки, окружённые липидной оболочкой, которую можно считать протомембраной. Понятно, что протомембрана, состоящая из синтезированных абиогенно липидов, ещё не содержала ни механических пор, ни полноценных белков, ни других мембранных атрибутов современной клетки, но она, тем не менее, уже обладала определённой избирательностью по проницаемости для различных простых органических и неорганических молекул. Одним из самых последовательных приверженцев подобного подхода является, в частности, нобелевский лауреат, американец, Джек Шостак. Автору данной статьи ближе гипотезы, подразумевающие очень раннее появление липидной мембраны, но для большей её правдоподонобности хорошо было бы найти какой-то конкретный механизм образования липидоподнобных молекул в условиях, благоприятных для протекания так же и ацетатного цикла, описанного выше.
В этом нам может помочь недавнее открытие способности нитрогеназ синтезировать из CO и водорода цепочки углеводородов (см. мою статью моя маленькая нитрогеназина). С момента завершения данной статьи прошло уже несколько лет, и за это время исследователи в деле изучения данного явления успели ощутимо продвинуться вперёд. В частности, было показано, что подобной же способностью обладает и так называемый L-кластер, имеющий химическую формулу Fe8S9C, и являющийся прекурсором (промежуточным звеном) при сборке ванадиевой и молибденовой нитрогеназ. Устройство L-кластера существенно проще, чем у активных центров созревших нитрогеназ, у него один из атомов железа ещё не замещён ванадием или молибденом, а так же ещё не присоединён гомоцитрат. Так вот, как выяснилось, даже в отсутствии белков "голый" L-кластер может восстанавливать угарный газ (CO) до углеводородов с длиной цепочки до 4-х атомов углерода, а цианид (CN) даже до углеводородов с длиной цепочки до 6-ти атомов углерода (CN - свободный радикал цианида был одной из первых молекул, обнаруженных в космосе, он образуется, например, при фотодиссоциации молекулы синильной кислоты под действием света). Правда, для этого нужен достаточно сильный восстановитель, однако, если, как предполагают многие исследователи, жизнь могла зародиться в пограничной зоне, отделяющей относительно кислую среду (например, воду на дне водоёма) от восстановленной (например, потоки горячей воды и раскалённых газов, поднимающиеся из верхних слоёв мантии), с ним, по идее, проблем было быть не должно.
Известно, что кристаллические структуры, подобные той, которая используется живыми системами при фиксации из внешней среды углерода (Fe4S4, Ni2S2 и т.д.) часто встречаются в неживой природе. А нет ли в ней и некого аналога обсуждаемого L-кластера? Оказывается, есть! L-кластер имеет много общего с кристаллами цементита, встречающимися в железных метеоритах (кстати, что характерно, часто железо в них частично замещено никелем и кобальтом, узок круг революционеров, совершивших прорыв от неживой материи!). Действительно, в цементите каждый атом углерода окружён шестью атомами железа подобно тому, как это реализовано в активном центре нитрогеназы. Далее, если элементарная ячейка цементита попадает в водную среду, богатую сероводородом (а он в ней непременно должен был быть, см. выше), сера будет активно реагировать с атомами железа, образовав поверх октаэдра, образованного его атомами, дополнительную внешнюю "шубу". Но ведь именно это мы и наблюдаем в кофакторе нитрогеназы! Находящиеся в ней поверх серной "шубы" два атома металлов по сути служат для фиксации активного центра внутри протеина, и хотя на итоговую каталитическую активность они, конечно, в какой-то мере влияют, тем не менее, факт возможной замены молибдена на ванадий или железо с сохранением потенциальной возможности фиксации азота косвенно говорит о том, что их роль, по-видимому, не является критически важной. Об этом же говорят и последние исследования, касающиеся механизма синтеза цепочек углеводородов нитрогеназами. Молекула угарного газа обратимо "оттирает" один из атомов серы, и становится на его место, образуя с помощью валентных электронов связи с двумя атомами железа, связанными, в свою очередь, с другими атомами серы и центральным атомом углерода. С "внешними" атомами металлов она, судя по всему, не реагирует. А теперь вспомним, что изолированный L-кластер способен синтезировать цепочки углеводородов длиной до 6-ти атомов углерода. Но ведь такие цепочки отличаются от простейших липидов, из которых могла, как предполагают, состоять архаичная мембрана самых первых организмов, всего лишь карбоксильной группой CO2(H) на одном из их концов (такие молекулы называют жирными кислотами). Учитывая, что производимый абиогенно ацетат (см. выше) по сути представляет из себя "карликовую" жирную кислоту с "хвостом", состоящим всего лишь из одного атома углерода, можно предположить, что используя те же минералы в качестве катализаторов, и подавая на вход CO и цепочки углеводородов небольшой длины ("хвост" которых, напомним, представляет из себя метильную группу CH3), мы можем получить на выходе не ацетат (или, скажем осторожнее, не только ацетат), но и жирные кислоты. Это так же косвенно подтверждается опытами по синтезу жирных кислот в условиях, примерно имитирующих условия для прохождения реакции Фишера-Тропша, но с добавлением карбоната калия K2CO3 (внимание, вот ещё одна важнейшая реакция, которую катализирует калий, немудрено, что в первичных клетках он был на вес золота!). В указанных опытах успешно синтезировались жирные кислоты длиной от 5 до 18 атомов углерода. Так как рассмотренный выше механизм синтеза цепочек углеводородов есть, по сути, всё тот же процесс Фишера-Тропша, но благодаря катализатором и использованию энергии окислительно-восстановительных реакций идущий при комнатых температуре и давлении, то вполне вероятно, что при подходящих, достаточно простых катализаторах (например, всё того же карбоната калия), можно добиться абиогенного синтеза не только углеводородов, но и жирных кислот. Дальше всё достаточно просто. Как показал в своих многочисленных опытах Д.Шостак, будучи представлены в водной среде в достаточной концентрации, жирные кислоты самопроизвольно собираются в мицеллы, а потом, при определённых условиях, и в простейшие структуры, напоминающие строение любой живой клетки (крошечные пузырьки жира, чем-то напоминающие мыльный пузырь, только в отличии от последнего, гидрофобные хвосты жирных кислот обращены внутрь, а не наружу, то есть, это как бы мыльный пузырь, вывернутый наизнанку) - везикулы. Вот на этом сайте можно ознакомиться с красочно оформленными дополнительными материалами по данной тематике.
Итак, из простейших и широко распространённых во Вселенной веществ (водород, сероводород, угарный газ, цианид) в присутствии в качестве катализаторов пород, содержащих, опять же, весьма распространённые в природе металлы (железо, никель, кобальт) и серу, на границе между окисленной и восстановленной средами, легко возникают цепочки химических реакций, приводящие не только к синтезу простой органики, но и к запасению свободной энергии в фосфатных связях, и даже образованию везикул, которые можно рассматривать как некий структурный прекурсор живой клетки, окружённой липидной мембраной. Дальше такие структурные единицы теоретически уже могут эволюционировать в плане отбора органических молекул и химических циклов, способных к самовоспроизводству. Например, если какая-то случайно синтезирующаяся в результате термодинамических флуктуаций молекула (аналог мутаций в биологии) будет способствовать запасению в системе свободной энергии, то это может увеличить вероятность её воспроизводства по принципу положительной обратной связи (сохранённая свободная энергия может использоваться для того, что бы ускорить синтез данной молекулы напрямую, не дожидаясь следующей подходящей флуктуации), так что концентрация подобных молекул в системе будет постепенно возрастать до тех пор, пока не сработают ограничения по доступности необходимого для её синтеза "сырья". Такую химическую систему, как уже говорилось выше, уже можно рассматривать как предтечу полноценной биологической системы, причём роль системной памяти в ней может играть сам набор "деталей" самовоспроизводящегося конструктора. Процессы слияния и разделения везикул будут способствовать возникновению между ними конкуренции за ресурсы, так что, до достижения какого-то порога устойчивости возможна эволюция системы в сторону усложнения. Подобную систему, состоящую из относительно простых органических молекул - аминокислот, нуклеотидоподобных молекул, липидов, и т.д., а так же незатейливых их комбинаций (скажем, широко распространённый кофермент SAM представляет из себя, по сути, сшитые вместе аминокислоту метионин и нуклеозид аденозин) можно рассматривать как своеобразный подготовительный этап к условному "миру РНК" (в реальности последний, по видимому, состоял не только из РНК, но и из коротких пептидов, фосфолипидов, тех же коферментов и т.д.).
Дальнейшая коэволюция как метаболических цепочек, так и поддерживающих их молекулярных комплексов, могла идти путём их пошагового усложнения. Скажем, исходно простая органика синтезировалась непосредственно на содержащих неорганические катализаторы породах (в первую очередь, включающих сульфиды железа и никеля), потом метильные группы стали синтезироваться на основе конденсирующегося на птерине формальдегида, потом и сам формальдегид стал синтезироваться непосредственно на птерине и т.д. до нынешней цепочки ацетогенов с CO2 и H2 на входе. В плане постепенного усложнения коферментов показательна вероятная эволюционная история нитрогеназы. Начаться она могла с того, что перед природой встала задача уменьшить зависимость от не столь широко распространённого цементита, синтезируя соответствующий катализатор самостоятельно. Решение было найдено в сборке аналога цементита из сырья, которое распространено гораздо шире - кубиков сульфида железа Fe4S4, входящих в состав широко распространённого грейгита. Пара таких кубиков вначале "сшивается" одним атомом серы, а потом метильная группа CH3 подвешивается на другой атом серы, после чего от неё один за другим отдираются ядра всех атомов водорода (задача, в некотором смысле обратная процессу, идущему при синтезе метильной группы, когда атомы водорода к углероду, наоборот, добавляются). В результате, атом серы избавляется от оставшегося в гордом одиночестве атома углерода, и ковалентно соединяется с двумя атомами железа из разных железно-серных кубиков (детали этого процесса до сих пор не до конца понятны и продолжают изучаться). В конечном итоге оба кубика оказываются прочно "пришиты" друг к другу двумя атомами серы, механическая конфигурация системы меняется, и атом углерода оказывается зажатым между шестью атомами железа. Вуаля, синтезированный минеральный кофермент можно доставлять в цех по производству простейших липидов. Некоторые подробности этого, всё ещё далеко не до конца изученного процесса, можно найти здесь. Со временем природа научилась синтезировать липиды гораздо более строго контролируя процесс с помощью довольно сложной цепочки, реализованной на основе кофермента А, и найденное красивое решение, возможно, так бы и затерялось за ненадобностью, но тут на счастье синтезируемая структура (тот самый упоминаемый выше L-кластер) оказалась востребованной при производстве ещё более сложной конструкции - нитрогеназы. Но природа не любит отступать от уже протоптанных тропинок. Соответственно, подобно тому, как у зародыша млекопитающих на ранних стадиях его развития проявляются, а потом исчезают, морфологические структуры, характерные для его предков (жабры и т.д.), так и в нашем случае вначале по уже "накатанной" цепочке синтезируется L-кластер, после чего он "апгрейдируется" путём замены одного из атомов железа на молибден или ванадий (хотя есть и исключение - редко использующаяся так называемая Fe-Fe нитрогеназа), и, главное, добавления к комплексу гомоцитрата (получившаяся в итоге конструкция известна как M-кластер). Итог всей этой героической эпопеи, тот самый M-кластер, в итоге безжалостно изымается от "родителей", то есть, из протеинового комплекса Nif(Vnf)EN, в котором он был собран (и может по прежнему вполне успешно работать в качестве катализатора для синтеза цепочек жирных кислот), и передаётся в другой комплекс, по видимому, произошедший от первого, и сохраняющий с ним существенную степень гомологии - Nif(Vnf)DK. С некоторыми подробностями описанных выше операций можно ознакомиться, например, здесь. Ну а полюбоваться крупным планом на результат работы слепого часовщика (хотя я бы лично, говорил не столько о часовщике, сколько о художнике), получившуюся в итоге одну из самых сложных минеральных структур, используемых живыми организмами, можно в соответствующей иллюстрации к статье А.Маркова на Элементах.
Ещё одной "головной болью" природы в процессе строительства живых систем было обеспечение достаточной их автономности, уменьшение зависимости от влияния внешних факторов. Например, водород, это, вообще говоря, очень ценный для живых систем газ, за доступ к нему у них всегда существует высокая конкуренция. Но поток водорода из глубинных пород, как правило, неравномерен, хорошо бы иметь возможность как-то запасать его "на чёрный день". В принципе, при наличии угарного газа, эта задача решается, в каком-то смысле, сама собой. Дело в том, что растворённый в воде CO неизбежно с ней реагирует по схеме CO + H2O <=> CO2 + H2. То есть, часть молекул угарного газа обратимо окисляется до углекислого с выделением молекулярного водорода. Данный процесс меняет общую свободную энергию Гиббса участвующих в нём молекул очень незначительно, поэтому он может идти как в ту, так и в другую сторону. В итоге, через какое-то время в системе устанавливается равновесие (лишь бы был в достатке угарный газ). Одна из причин ценности водорода заключается в том, что его довольно легко "разобрать" на протон и электрон, которые потом могут использоваться в различных метаболических процессах. Осуществлять окисление (как, впрочем, и восстановление) водорода умеют специальные ферменты, так называемые гидрогеназы. Как Вы, вероятно, уже догадались, в их активном центре находится нехитрая конструкция, состоящая всё из тех же атомов никеля и/или железа. Обычно, это два атома металла(ов), соединённых вместе двумя атомами серы, и дополнительно "обвешенные" всё теми же вездесущими молекулами CO и CN. Любопытно, что если Ni-Fe вариант работает преимущественно в направлении окисления водорода, то вариант Fe-Fe, наоборот, его по большей части восстанавливает из электронов и протонов. Таким образом, подавляя активность минерального кофермента того или иного типа (кстати, работа Ni-Fe центра ингибируется повышенной концентрацией в среде всё того же CO!), можно в какой-то мере регулировать как концентрацию водорода, так и степень кислотности среды.
Обобщая вышеизложенное, можно представить себе следующий примерный сценарий развития событий. Первые самоподдерживающиеся химические (протометаболические) циклы возникли при взаимодействии растворённых в воде газов, таких, как CO, H2, H2S, NH3 (NH4+) между собой в присутствии в качестве катализаторов пород, содержащих такие химические элементы, как железо, никель, кобальт, сера. При этом, часть CO реагировала с водой, частично (и обратимо) превращаясь в водород и углекислый газ. Это обстоятельство способствовало поддержанию в среде определённой концентрации такого удобного восстановителя, как свободный водород, который, в свою очередь, по мере необходимости, мог частично окисляться до протонов и электронов природными катализаторами - гидрогеназами, включающими серу, железо и никель. Возникающие химические циклы и первые органические молекулы проходили естественный отбор на выживаемость в процессах автокаталитического воспроизводства (за счёт положительных обратных связей) и стабилизации (за счёт отрицательных обратных связей). Возможно, определённую роль в возникновении жизни сыграл и предложенный автором в одной из предыдущих статей вариационный принцип "усиления" второго закона термодинамики. Любая замкнутая система не просто всегда эволюционирует к состоянию с максимальной энтропией, но и выбирает при этом из всех возможных траекторий такую, при которой это конечное состояние достигается наиболее быстро. Живые организмы в каком-то смысле ускоряют эволюцию термодинамической системы, катализируя реакции, которые приводят в итоге к тем же результатам, какие были бы достигнуты и без их участия, но за гораздо больший промежуток времени. Дальнейшая эволюция живых систем шла в направлении поиска более надёжных носителей для запоминания удачных флуктуаций (РНК-ДНК), и добавления дополнительных шагов в уже сложившиеся протометаболические циклы.
