Противораковые препараты
Статьи в тематическом сборнике являются авторскими и могут не отражать направленность сайта.
Противораковые препараты (антионкологические средства) применяются для лечения злокачественных опухолей. Они воздействуют на быстро делящиеся клетки, в том числе на раковые. Как пример противоракового препарата - абиратерон имеет цену, приемлемую для больных и доступен во многих аптеках. Это важный и эффективный противораковый препарат, применяемый при лечении гормонозависимых опухолей, в частности — рака предстательной железы. Он относится к ингибиторам синтеза андрогенов.
Абиратерон подавляет фермент CYP17 (17α-гидроксилазу/С17,20-лизазу), который участвует в синтезе андрогенов (в том числе тестостерона) не только в яичниках или яичках, но и в надпочечниках и непосредственно в раковой ткани простаты.
Таким образом, он снижает уровень всех источников андрогенов, что особенно важно при кастрационно-резистентном раке простаты (КРРП) — когда опухоль продолжает расти даже при очень низком уровне тестостерона.
В зависимости от механизма действия выделяют несколько основных видов противораковых препаратов:
Цитостатики (цитотоксические препараты)
Это классические химиотерапевтические средства, которые подавляют рост и деление клеток. Есть несколько подвидов цитостатиков:
Алкилирующие агенты
Примеры: Циклофосфамид, Цисплатин, Карбоплатин
Механизм: Повреждают ДНК, предотвращая деление клеток.
Антиметаболиты
Примеры: Метотрексат, 5-фторурацил, Гемцитабин
Механизм: Имитируют структуры веществ, необходимых для синтеза ДНК, блокируя её производство.
Антрациклины
Примеры: Доксорубицин, Эпирубицин
Механизм: Повреждают ДНК и ингибируют фермент топоизомеразу II.
Митозные ингибиторы (препараты растительного происхождения)
Примеры: Параклитаксел, Доцетаксел, Винкристин, Винбластин
Механизм: Нарушают формирование веретена деления, останавливая митоз.
Топоизомеразные ингибиторы
Примеры: Иринотекан, Топотекан, Эттопозид
Механизм: Блокируют ферменты, участвующие в раскручивании ДНК, что приводит к разрывам цепочек.
Таргетные препараты (таргетная терапия)
Действуют на специфические молекулы или рецепторы, связанные с ростом опухоли.
Примеры:
Ингибиторы тирозинкиназ
Примеры: Иматиниб, Лапатиниб, Эрлотиниб, Гефитиниб
Механизм: Блокируют сигналы, стимулирующие рост опухолевых клеток.
Ангиогенез-ингибиторы
Примеры: Бевацизумаб, Сорафениб, Сунитиниб
Механизм: Останавливают образование новых кровеносных сосудов, питающих опухоль.
АнтиртГФ-β (антирецептор трансформирующего фактора роста бета)
Примеры: Радотрикс (на примере онкологического заболевания — кожный Т-клеточный лимфомы)
Гормональные препараты
Используются при гормонозависимых опухолях (например, рак молочной железы, рак простаты).
Примеры:
Ингибиторы ароматаз: Анastroзол, Летрозол
Антиэстрогены: Тамоксифен
Аналоги ЛГРГ (гонадотропин-рилизинг гормона): Гозерелин, Лейпрорелин
Антиандрогены: Бикалутамид
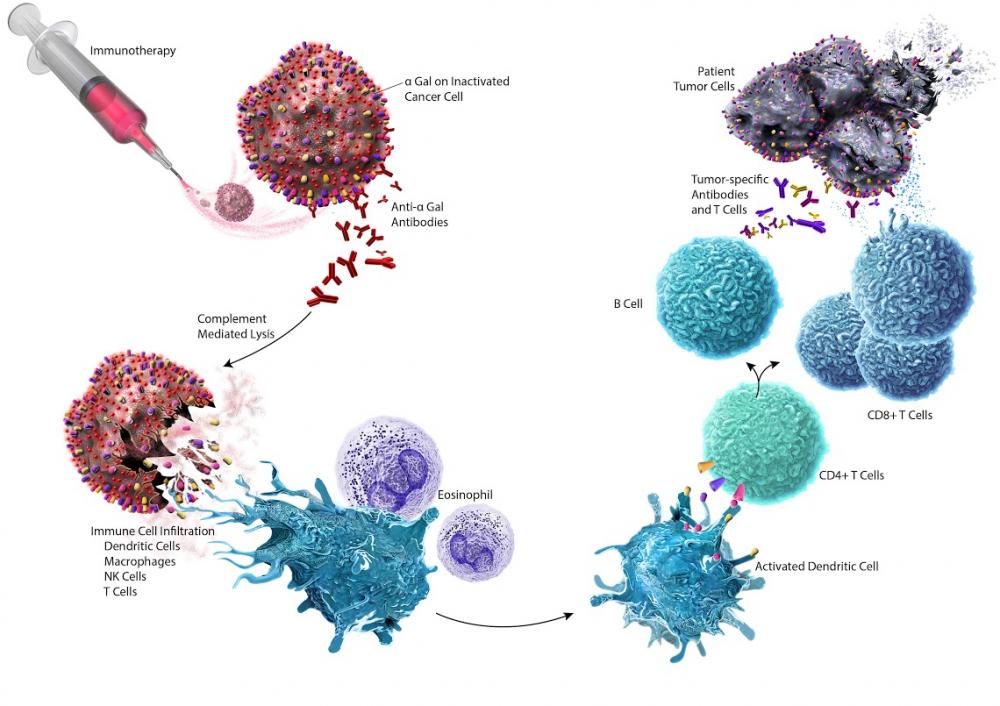
Иммунотерапия
Повышает способность иммунной системы распознавать и уничтожать раковые клетки.
Примеры:
Ингибиторы контрольных точек иммунитета (checkpoint inhibitors)
Примеры: Пембролизумаб, Ниволумаб, Ипилимумаб
Механизм: Убирают "тормоза" иммунного ответа, позволяя Т-лимфоцитам атаковать опухоль.
CAR-T-клеточная терапия
Примеры: Кимриах, Язультта
Механизм: Изменённые иммунные клетки пациента уничтожают определённые виды раковых клеток.
Цитокины
Примеры: Интерфероны, интерлейкины
5. Препараты радионуклидной терапии (радиоиммунотерапия)
Содержат радиоактивные изотопы, направленно поражающие опухоль.
Примеры:
Иод-131 (при раке щитовидной железы)
Лутетий-177 (например, Lutathera при нейроэндокринных опухолях)
6. Противоопухолевые антибиотики
Хотя не все они являются антибиотиками в традиционном понимании, это группа препаратов, полученных из микроорганизмов.
Примеры:
Блеомицин
Даунорубицин
Бисфосфонаты и деносумаб
Не убивают раковые клетки напрямую, но помогают при метастазировании в кости.
Примеры:
Золедроновая кислота
Деносумаб
Выбор препарата зависит от типа опухоли, её стадии, наличия молекулярных маркеров, общего состояния пациента и других факторов. Часто используются комбинированные схемы, включающие несколько групп препаратов.
Перспективы разработок новых высокоэффективных препаратов
Развитие онкологии в последние десятилетия связано с бурным прогрессом в области фармацевтики и молекулярной биологии. Современные исследования направлены на создание новых, более эффективных и менее токсичных препаратов , способных обеспечить длительный контроль над опухолью и даже излечение при некоторых формах рака.
Таргетная терапия: персонализированный подход
- Разработка препаратов, направленных на конкретные генетические мутации (например, ингибиторы BRAF, ALK, ROS1, MET, RET).
- Препараты третьего поколения для пациентов с устойчивостью к предыдущим терапиям (например, осимертиниб при мутациях EGFR).
- Универсальные "пан-мутационные" препараты, такие как ларотректиниб и ентректиниб , действующие независимо от локализации опухоли.
Иммунотерапия: будущее противоопухолевого иммунного ответа
- Расширение применения ингибиторов контрольных точек (PD-1/PD-L1, CTLA-4) на новые виды рака.
- Разработка би- и три-специфических антител , усиливающих связь между Т-клетками и опухолевыми клетками.
- CAR-T-клеточная терапия выходит за рамки гемобластозов и тестируется при твёрдых опухолях.
- Вакцинотерапия — персонализированные антиген-специфические вакцины на основе мутанома опухоли (например, mRNA-вакцины).
Пролекарства и доставка лекарств
- Использование антителосопряжённых препаратов (ADC) , которые доставляют цитотоксин прямо в опухоль (например, энфоружин, трастузумаб дерукстекан ).
- Нанотехнологии и липосомальные формы для повышения специфичности и снижения системной токсичности.
Комбинированное лечение
- Комбинации таргетных препаратов с иммунотерапией или химиотерапией для преодоления резистентности.
- Исследования по использованию метаболических модуляторов и ингибиторов ДНК-репарации в сочетании с другими методами лечения.
Фармакогеномика и персонализированная медицина
- Определение молекулярного профиля опухоли позволяет подбирать наиболее эффективную терапию.
- Выявление предикторных биомаркеров (PD-L1, TMB, MSI, BRCA и др.) помогает прогнозировать ответ на лечение.
Натуральные соединения и новые химические структуры
- Поиск активных веществ в природных источниках (морские организмы, растения).
- Использование искусственного интеллекта и компьютерного моделирования для ускоренного скрининга молекул с потенциальной противоопухолевой активностью.
Упрощение терапии и улучшение качества жизни
- Создание пероральных аналогов инъекционных препаратов .
- Разработка долгоиграющих форм с меньшей частотой введения.
- Минимизация побочных эффектов за счёт высокой селективности действия.
Благодаря достижениям в области геномики, биотехнологии и цифровых технологий, сфера разработки противораковых препаратов стремительно развивается. Будущее онкологического лечения — за точной, целевой и комбинированной терапией , основанной на индивидуальном профиле опухоли пациента. Это открывает новые горизонты в борьбе с раком, превращая его из неизлечимого заболевания во всё более контролируемое хроническое состояние.